Wat is Thermodynamica?
De thermodynamica houdt zich bezig met allerlei soorten energieomzettingen. Deze is ontstaan in de tijd dat men zich bezighield met de omzetting van warmte in kracht. Het woord thermodynamica is dan ook afkomstig van de Griekse woorden ‘therme’ (warmte) en ‘dynamis’ (kracht). Thermodynamica wordt gebruikt bij de analyse en het ontwerp van apparaten. (bron: TU Delft)
De eerste hoofdwet van Thermodynamica:
De wet van behoud van energie wordt ook wel de eerste hoofdwet genoemd, maar feitelijk is de eerste hoofdwet gebaseerd op de wet van behoud van energie. Volgens de wet van behoud van energie geldt: energie kan niet uit het niets ontstaan en ook niet verloren gaan.
De tweede hoofdwet van Thermodynamica:
De tweede hoofdwet heeft te maken met de richting van waar de energie heen gaat. Zo zal warmte van warme naar koude voorwerpen stromen en niet andersom. Een andere formulering van de tweede hoofdwet is dat het onmogelijk is om met een terugkerend proces de warmte die door een systeem geabsorbeerd wordt volledig in arbeid om te zetten. Er gaat dus altijd ergens energie aan verloren.
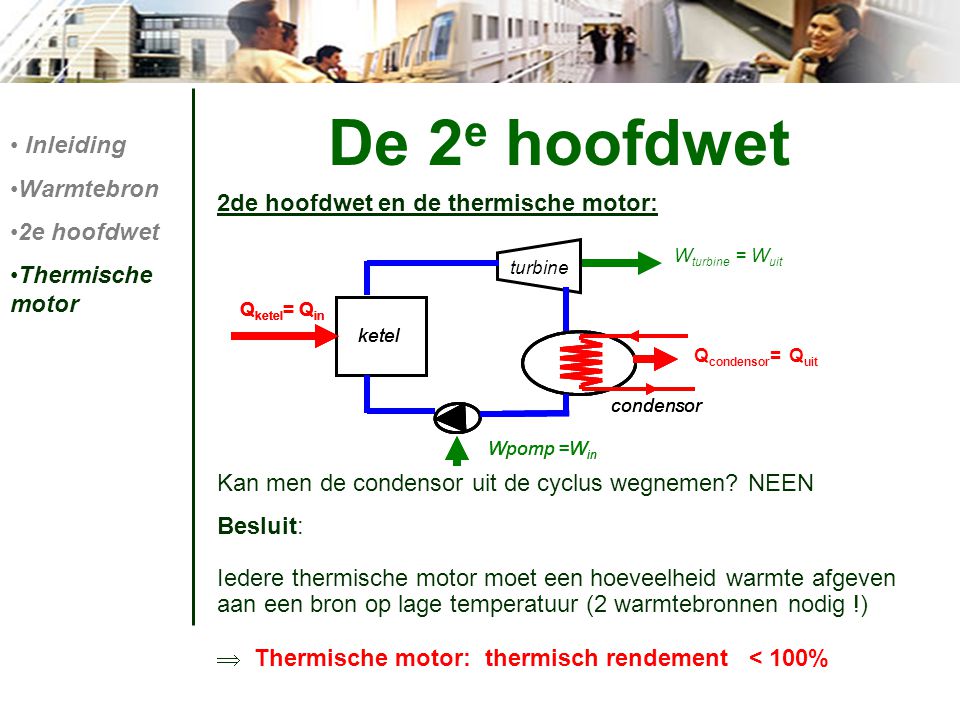
2de hoofdwet en de thermische motor: Kan men de condensor uit de cyclus wegnemen? NEEN. Besluit: Iedere thermische motor moet een hoeveelheid warmte afgeven aan een bron op lage temperatuur (2 warmtebronnen nodig !) Thermische motor: thermisch rendement < 100% Wturbine = Wuit. turbine. Qketel= Qin. Qketel= Qin. Qketel= Qin. ketel. ketel. ketel. Qcondensor= Quit. condensor. condensor. condensor. Wpomp =Win. Wpomp =Win. Wpomp =Win.
In werkelijkheid is de entropieverandering altijd groter dan nul. Alleen bij denkbeeldige processen die omkeerbaar verlopen is de entropieverandering gelijk aan nul. Deze denkbeeldige processen worden omkeerbare processen genoemd.
Dan is er ook een ‘nulde (0-de) hoofdwet’:
De nulde hoofdwet is van een groter belang dan de eerste en tweede hoofdwetten, maar werd later in woorden omgezet (geformuleerd) en is daarom de nulde hoofdwet genoemd. Deze nulde hoofdwet stelt dat wanneer twee systemen in thermisch evenwicht zijn met een derde systeem (= dezelfde temperatuur hebben), zij ook in thermisch evenwicht met elkaar zijn. Dit filmpje legt uit wat ‘thermische energie’ is.
De derde hoofdwet heeft te maken met het absolute nulpunt van de temperatuur, -273,15 °C. Bij dat absolute nulpunt zijn moleculen bewegingloos en is er geen onduidelijkheid meer over waar moleculen zich bevinden, m.a.w. er is geen wanorde meer. De formulering van de derde hoofdwet van de thermodynamica is dan ook: de entropie van een zuivere kristallijne stof bij het absolute nulpunt is nul.

